Endale selgema ülevaate saamiseks hakkasin tõlkima Potsdami
Ülikooli kursuse „Molecular Basis of Nutriton Related Diseases“ (toitumisega
seotud haiguste molekulaarsed alused) materjale. Kursusest endast võid lugeda
täpsemalt Iversity kodulehelt.

Tegemist ei ole taimetoitlasest professoriga ega
veganitest teadlastega:). Ja taimetoidust juttu ei tulegi:). Kuid tähelepanelikult lugedes seda materjali, võid
leida palju ilmselgeid seoseid ja aru saada, kuidas me sellele diabeedi,
ateroskleroosi, düslipideemia teele oleme läinud ja jäänudki.

Kursuse esimene osa on suhteliselt lihtsalt mõistetav.
Et seda veelgi illustreerida, võiks küsida, mis juhtub pilgeni täis
riidekapiga, kuhu topitakse veel paar kasti riideid? Mis juhtub
raamaturiiuliga, kui sinna laotakse juurde aina uusi raskusi? Kui garaaž on
mõeldud 2 autole, siis kas tundub arukas võtta kuvalda ja press ning toppida
sellesse garaaži 10 autot? Kui sul on hea elada koos ühe elukaaslasega, kas 25
elukaaslast sinuga ühes toas oleks meeldiv? Umbes nii me teemegi oma kehaga.
Looduses on saadaval ainult suhteliselt lahja toit. Lahja toit annab keskmiselt
energiat. Võib-olla isegi vähe energiat. Kuid tegelikult piisavalt, et saada
enda käsutusse jõud, mis ei kurna liigselt. Sa ei saa piisavalt energiat
selleks, mida sa nii meeletult tahad. Kuna sa tahad seda, mida sul ei ole ja sa
tahad seda, mis sul on, palju-palju-palju rohkem. Sestap anname kehale ka energiat
palju-palju-palju rohkem. Me oleme õppinud tegema ka sellist toitu, mis pakatab
meeletust energiast. Õun on lahja, mahub peopessa. Võipakk mahub ka. Mis on
või? Lehm ca 500 kg sünnitab vasika ca 31 kg. Vasikas joob päevas 8 liitrit
piima (sunnitud piirang) ja vabalt valides ca 12 liitrit piima ning kaalub 9
kuuselt 250-270kg. St võtab kuus juurde kuni 36 kg. 9 kuuselt on lehm valmis andma uut järglast. Või
sisaldab 80% rasva ja 3,25% piima kohta tuleb – 10 liitrit piima annab 0,39
liitrit võid. Selle koguse võid söövad paljud saiakestes, pitsades,
praetoitudes ära mitu korda päevas. Õli-margariini puhul ei ole vahet –
kalorsus on rasva puhul meeletu energia. Võimalus olla veel parem, saada veel
rohkem.

Järgnevate tõlgete puhul koorub välja tegelikult ka
see, miks tänapäevane diabeedi ravi mingit tulemit ei anna ja ei saagi anda. Loodus
andis meile insuliini ja kogu selle energia talletamise-vabanemise protsessi looduses
elamiseks. See on sügavalt meie geenides – nii märgivad edaspidi viidatavad
uuringud ja paljud teadlased. Looduses käib vaheldumisi toidu rikkus ja toidu
vaegus. On ajad, mil toitu on külluses, siin on abiks insuliin. On ajad, mil
toitu on väga vähe. Ja kõik toimib – sestap metsloomad ei ole diabeedis. Nad saavad
vahel palju süüa, kuid on aegu kus on päris pikk paast. Ülesöönud kodukassid ja –koerad aga juba on
diabeedis. Lakkamatu ja pidev söömine – igapäevane pidulaud. Ei mingit suurt
energiakulu selle kättesaamisel. Igapäevane kümnekordselt kokkupressitud rasva-valgu-rafineeritud
süsivesiku energiapomm. Keha lõpetab insuliini tootmise, kuna energiat on
liiast. ß-rakk sureb välja, kuna jätkuv hullumeelne energiavoog ei paistagi
lõppevat. Ja me vaevame pead selle üle, miks pankreas enam beeta rakke ei
tooda! Kuidas ta saakski – ei ole ju vajadust, ei ole looduslikku vähesust. Mitte
keegi isegi ei püüa ravida oma diabeeti sellega, et sööks vähem ja palju vähem
kontsentreeritud toitu. Liiguks enam. Meie keha geneetikaga on kõik korras. See
toimib suurepäraselt. Mida rohkem, seda uhkem
– see vanasõna on nüüd oma lae saavutanud (võib-olla) ja diabeedi puhul peaks
elama vastupidise sõnaga – mida vähem, seda parem.
Prof. Gerhard Püchel Pottsdami Ülikoolist:
Meie aju ei ole ainult koht, millega me mõtleme; aju
kontrollib paljusid elulisi funktsioone kehas. Korralikuks tööks vajab keha
glükoosi – konstantselt. Glükoosist toodetakse ATP (Adenosiintrifosfaat ehk adenosiin-5’-(tetravesinik
trifosfaat) ehk ATP on universaalne energia talletaja ja ülekandja, mis osaleb
kõigirakkude metabolismis.
ATP on makroergiline ühend. ATP-d toodetakse kõige
rohkem mitokondrites.), mis annab energiat närvirakkude rakufunktsioonide
tarbeks. Aju korralikuks funktsioneerimiseks on vajalik vere glükoositaseme
teatud kindel miinimum. Ja alla selle kriitilise miinimumi langemine toob kaasa
surma.
Glükoosi saame omale
toidust. Normaalse toidukorra puhul saame glükoosi palju rohkem, kui keha
akuutselt vajab. Glükoosi ülejääki
säilitatakse glükogeenina maksas.

Toidukordade vahel, mil väljastpoolt
glükoosi kehasse ei tule, kasutatakse seda varu, et aju saaks glükoosi. Kui
glükoosi tuleb kehasse pidevalt suures koguses, siis on ka skeletilihas võimeline
säilitama suurel hulgal glükoosi glükogeeni vormis. Kuid erinevalt maksast, ei
suuda lihas anda glükoosi verre, et pakkuda ajule energiat.
Võib arvata, et siis
tasub hoida vere glükoositase nii kõrgel kui võimalik, et ajul oleks energia
kindlustatud. Lühiajaliselt ei ole kõrge glükoositase tervisele ilmtingimata
ohtlik, kuid pikemas perspektiivis on ta seda aga küll. Seega peab glükoosi
tase olema optimaalne. Hormooni, mis
takistab vere glükoositaset tõusmast üle optimaalse, nimetatakse insuliiniks.
Insuliini toodab pankrease ß-rakk ja insuliin vabaneb verre, kui vere
glükoositase tõuseb. Glükoos stimuleerib insuliini vabanemist pankreasest.
Insuliin aga omakorda stimuleerib glükoosi tootmist glükogeeniks nii maksas,
kui skeletilihastes ning inhibeerib (takistab) glükoosi vabanemist maksast.

Meie toit sisaldab
rasva. Kui aju välja jätta, siis suudavad paljud organid toota omale energiat
(ATP) rasvas leiduvate rasvhapete oksüdeerimisel. Kui rasvhappeid tuleb kehasse
rohkem keha otsesest vajadusest, siis rasvhappeid säilitatakse triglütseriidide
vormis rasvkoes. Sealt võib toidukordade vaheajal energiat mobiliseerida.
Insuliin stimuleerib rasvhapete triglütseriidide vormis rasvkoes säilitamise ja
inhibeerib (takistab) sellest laost rasvhapete vabanemist. Vastupidiselt
glükogeeni laole võib triglütseriidide ladu tohutult kasvada – seda juhul, kui
energia juurdevool ületab pidevalt energia vajaduse. Tekib ülekaal ja edasi
rasvumine.

Kui rasvkude ületab oma
tervislikud piirid, siis hakkab ta häirima ainevahetuse protsesse. Täpsemalt –
rasvkoest vabanevad mediaatorid ja substraadid, mis kahjustavad insuliini
funktsioone skeletilihastes ja maksas. Kuigi insuliin ringleb veres, ei saa ta
enam stimuleerida glükoosi muutmist glükogeeniks ega ka inhibeerida glükoosi
vabanemist maksast. Lihas, maks ja samuti ka rasvkude ise muutvad nö insuliini
resistentseks.
Selle tulemusena hakkab
tõusma vere glükoositase. Pankreas püüab kompenseerida insuliini resistentsust
sellega, et toodab veel enam insuliini. Nii võib teatud ajaks vere glükoositase
olla normis – hoolimata insuliini resistentsusest. Kuid aastate jooksul ß-rakud
kahjustuvad sedavõrd, et ei suuda toota enam piisavalt insuliini, et insuliini
resistentsusega hakkama saada. Nüüd jääb vere glükoositase kõrgeks ja tekib 2
tüübi diabeet.
KUIDAS TEKIB INSULIINI
RESISTENTSUS?
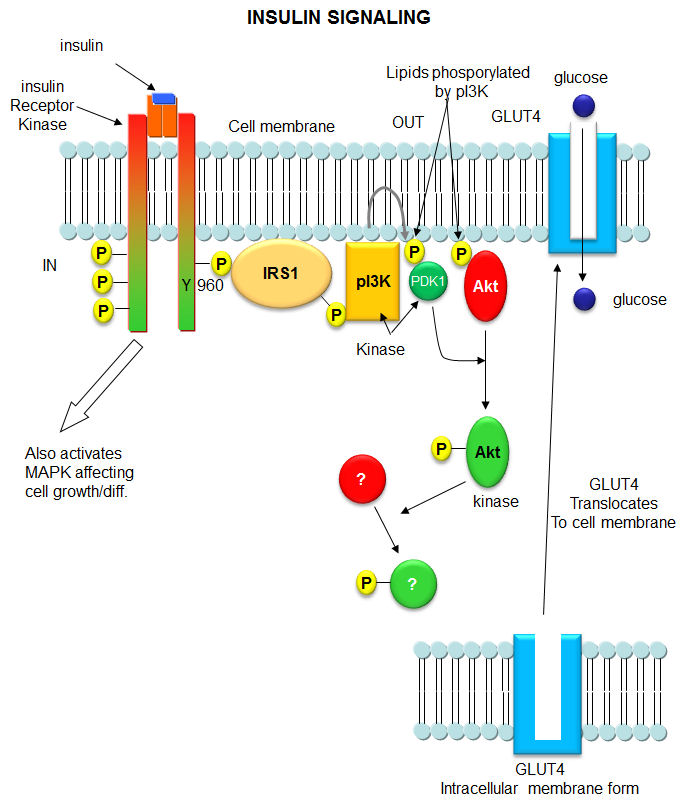
Et saada parem
ülevaade, vaatame lihtsustatud skeemi sellest, kuidas insuliin töötab
skeletilihases, maksas ja rasvkoes.
Insuliin on
proteiinhormoon, mis ei suuda rakku siseneda. Insuliinile tundlikud rakud
vajavad enne seega signaali raku pealispinnalt - selle signaali võtab vastu
insuliini retseptor, mis seob endaga insuliini ja laseb ta raku sisemusse, kus
insuliin saab osa võtta raku funktsioonidest. Rakusisene signaalahel
aktiveeritakse – see hõlmab endaga mitmeid erinevaid valke plasma membraani
sisepinnal. Signaal nö levib mööda seda valgulist ahelat ja oma struktuuri
kergelt muutes toimub ahela aktiveerumine. Sellise signaalahela eesmärk on
võimendada signaali ja anda edasi täpsem informatsioon. Ahela lõpus
aktiveeritakse ensüümid, mis moduleerivad järgmiste valkude funktsioonid –
näiteks: seovad enda külge fosfaadi (seda ensüümi teatakse, kui valgu
kinaas ingl.k protein kinase http://et.wikipedia.org/wiki/Proteiinkinaasid
). Üks olulisi kinaase kannab nime Akt kinaas. See kinaas on vastutav
suurenenud glükoosihulga vastuvõtu eest skeletilihasesse, suurenenud glükogeeni
sünteesi eest maksas ja skeletilihases ja suurenenud triglütseriidide sünteesis
rasvkoes.
Kui rakud on energiaga
üle ujutatud ja seega ei tohiks endasse
enam võtta rohkem energiat, siis nad hakkavad andma signaale, mis nö eraldab
signaalahela insuliini retseptorist. Samuti saavad rakud vastu võtta insuliini
vastuvõtmise lõpetamise signaali teistelt rakkudelt. Paljud rakud, mis on
seotud kudedes põletiku tootmisega, toodavad selliseid signaale. Ei ole oluline, kas signaal tuleb raku
seest- või väljastpoolt - insuliini
retseptori signaalahel katkeb. Toimub see kahel viisil: kas signaalahela
kahe valgu vahel signaali edasi andmine peatub või nõrgeneb signaalahela ühes
valgus signaali edasikandumine. Insuliin suudab ennast edasi siduda insuliini
retseptori külge raku välispinnal, kuid kuna signaal puudub, kinaas ei vabane.
Rakk on muutunud insuliini resistentseks.
KUIDAS INSULIINI RESISTENTSUS
MÕJUTAB ERINEVAID KUDESID?
Rasvarakkudes
stimuleerib insuliin rasvhapete ladustamist triglütseriidide lattu ja
inhibeerib (takistab) sellest laost rasvhapete vabanemist. Ilmselgelt on
rasvkoe laienemine kogu keha insuliini resistentsuse lähtepunkt ning rasvkude
ongi esimene koht, kus insuliini resistentsus välja areneb. See hõlmab endas
juba eelnevalt kirjeldatud mehhanismid: adipotsüütide (ingl. k. Adipocytes - teatud ka
kui lipotsüüdid ja rasvarakud – on rakud, millest peamiselt koosneb rasvkude;
need rakud on spetsialiseerunud energia säilitamisele rasvana)
ülekoormamine triglütsertiididega tekitab signaalid üleliigse energiakoguse
osas. Osad adipotsüüdid, mis on endasse aplalt lipiide ahminud, surevad ja
tekib lokaalne madalama astme põletik. Mõlemad signaalid: nii üleliigse
energiakoguse, kui ka põletiku omad lõhuvad insuliini signaalahela
rasvarakkudes ning rasvarakud muutvad insuliini resistentseks. Insuliinile
resistentne rasvarakk enam rasvhappeid ei säilita. Pigem nad vabastavad
rasvhapped, et varusid vähendada, kuigi keha ülejäänud koed täiendavat energiat
ei vaja. Rasvhapete väljavool rasvarakkudest keha teistesse kudedesse suureneb
ja teiste kudede koormus sellega toime tulla kasvab.
Mis juhtub maksas ja
skeletilihases, kui nad saavad rasvhappeid rohkem, kui tavapärase metabolismi raames vaja?

Skeletilihasel
on kaks viisi toota ATP-d: ta võib põletada glükoosi anaeroobses ja aeroobses
glükolüüsis või ta põletab rasvhappeid. Kui glükoosi on külluslikult, siis
skeletilihas võib üles ehitada glükogeeni lao. Insuliin stimuleerib glükoosi
säilitamist glükogeeni vormis. Igal juhul on reegliks, et skeletilihases
ladustatakse rasvhappeid triglütseriidide vormis vähe või üldse mitte. See aga
muutub, kui rasvkoe düsfunktsioneerimise tulemusena jõuab lihaseni järjepidev
ülemäärane rasvhapete kogus. Skeletilihas hakkab üles ehitama ladu, mida
nimetatakse ektoopiliseks ( ektoopiline rasv defineeritakse kui
triglütseriidide depoo mitte-rasvkoe rakkudes, mis normaalselt sisaldavad
ainult väga väheses koguses rasva) triglütseriidide laoks. Nüüd loob
ektoopiline triglütseriidide ladu energia ülekülluse signaalid, mis lõhuvad
insuliini signaalahela. Siitsamast tekibki hüperglükeemia, eriti peale
toidukordi.

Maksal
on täita väga palju funktsioone ja ta teenindab kogu keha. Üks olulisim
funktsioon on olla puhver: säilitada liigset glükoosi ja anda vajadusel
glükoosi välja, sealhulgas ajule.
Insuliin reguleerib seda funktsiooni, suurendades glükoosi varusid ja
inhibeerides (takistades) glükoosi vabanemist. Lisaks sellele mängib maks
olulist rolli lipiidide metabolismis (ainevahetuses). Ta pakib lipiidid ümber
nii, et teistel kudedel oleks neid parem kasutada ja suudab isegi liigse koguse
süsivesikuid muuta rasvhapeteks. Normaaljuhul maks ei ladusta suuremat kogust
lipiide. Ja jällegi – see muutub, kui rasvhapete kogus aina kasvab. Maksarakud
akumuleerivad triglütseriidid. Areneb
välja rasvunud maks. Selline triglütseriidide akumuleerimine rikub
maksaraku normaalset funktsioneerimist. Nii nagu skeletilihaseski katkeb
insuliini signaalahel energia ülekülluse signaalide tõttu. Lisaks sellele,
mõned lipiididega täitunud maksarakud surevad ja tekib lokaalne madala astmega
põletik. See loob täiendavad signaalid, mis samuti katkestavad insuliini
signaalahela maksarakkudes. Tagajärjeks on, et insuliin ei saa enam peale sööki
stimuleerida glükoosi ladustamist maksas ja ei saa ka toidukordade vahel
takistada maksas liigse glükoosi tootmist. Tagajärjeks on kõrgem glükoositase
veres.

Rasvkoe
düsfunktsioneerimine ülekaalus ja rasvunud inimestel võib mõjutada insuliini
tegevust maksas ja skeletilihases veel ühel moel: terve rasvkude vabastab
hormoone, mis aitavad insuliinil suurendada glükoosi utiliseerimist maksast ja
skeletilihasest. Üks sellistest hormoonidest on adiponektiin. Seda hormooni
toodab terve adipotsüüt. Kui triglütseriidide ladu adipotsüüdis kasvab, siis
adiponektiini tootmine väheneb. Kui adiponektiini tase väheneb, väheneb
skeletilihasest ja maksast utiliseeritava glükoosi hulk. Adiponektiini koguse
vähenemine viib terve keha insuliini resistentsuse arenguni....
Selleks korraks on juba piisavalt pikk tekst. Mingil ajal (kui on vihmane ja aed ei kutsu), läheb see kõik edasi, aina sügavamale ja sügavamale. Ma siin muidu mõtisklen, et hoolimata energia üleküllusest ja liig ravsasest toidust ostame apteekidest ja tervisepoodidest head rasva aina lisaks:).
